MODELOS ATÓMICOS
MODELO ATÓMICO DE THOMSON
J. J. Thomson, en 1897, demostró que al aplicar un campo eléctrico los rayos que viajaban del cátodo al ánodo eran desviados hacia la placa positiva, lo que hacía suponer que los rayos catódicos poseían carga negativa.
También demostró que estos rayos poseían naturaleza corpuscular, es decir, estaban formados por partículas. A estas partículas negativas Thomson las llamó electrones.
A pesar del gran avance de Thomson, él no pudo encontrar de forma ndependiente la carga y la masa del electrón. Pero descubrió la relación que existe entre la masa y la carga de esta partícula.
¿Cuál es el valor de la relación carga-masa del electrón?
Thomson hizo otro descubrimiento importante. Demostró que la naturaleza de los rayos catódicos era independiente del material del que estaba hecho el cátodo. Llegó entonces a la conclusión de que los electrones eran partículas constitutivas de toda la materia.
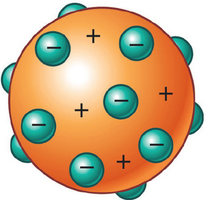
En 1904, J. J. Thomson ideó un modelo atómico, en el cual sugiere que el átomo es una esfera con carga positiva, la cual estaba uniformemente distribuida en todo el átomo. Los electrones se encuentran embebidos en el átomo, en cantidad necesaria para neutralizar la carga positiva. Este modelo se asemeja a las pasas en un budín, por lo cual se le conoce con este nombre.